Նյութերի գազային ագրեգատ վիճակի թերմոդինամիկան ֆիզիկայի կարևոր ճյուղ է, որն ուսումնասիրում է թերմոդինամիկական հավասարակշռությունը և քվազաստատիկ անցումները համակարգերում։ Հիմնական մոդելը, որի վրա հիմնված են համակարգերի վարքագծի կանխատեսումները, իդեալական գազի մոդելն է: Դրա կիրառմամբ ստացվել է Մենդելեև-Կլապեյրոն հավասարումը։ Հաշվի առեք այն հոդվածում։
Իդեալական գազ
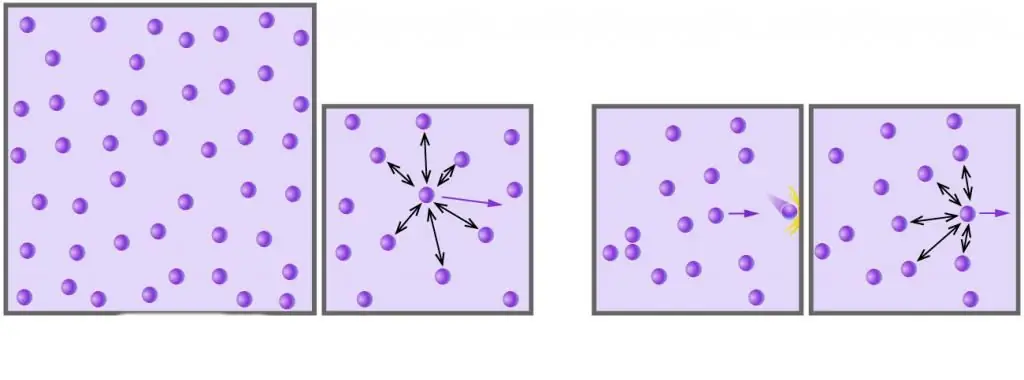
Ինչպես գիտեք, բոլոր իրական գազերը բաղկացած են մոլեկուլներից կամ ատոմներից, որոնց միջև հեռավորությունները չափազանց մեծ են՝ համեմատած ցածր ճնշման դեպքում: Բացի այդ, բարձր ջերմաստիճաններում, բացարձակ մասշտաբով, մոլեկուլների կինետիկ էներգիան գերազանցում է նրանց պոտենցիալ էներգիան՝ կապված թույլ դիպոլ-դիպոլ փոխազդեցությունների հետ (եթե, բացի այդ փոխազդեցություններից, կան նաև այլ տեսակի քիմիական կապեր, օրինակ՝ իոնային կամ ջրածինը, այնուհետև նրանք զգալի ներդրում ունեն ներքին համակարգի էներգիայի պոտենցիալ բաղադրիչի մեջ):
Պայմանավորված էՇատ իրական գազերի համար նորմալին մոտ պայմաններում կարելի է անտեսել նրանց ներքին փոխազդեցությունները և մասնիկների չափերը: Այս երկու հիմնական մոտարկումները կազմում են գազի իդեալական մոդելը։
Մենդելեևի հավասարումը ֆիզիկայում

Ավելի ճիշտ և արդարացի է այս հավասարումն անվանել Կլապեյրոն-Մենդելեև օրենք: Բանն այն է, որ այն առաջին անգամ գրանցել է ֆրանսիացի ինժեներ Էմիլ Կլապեյրոնը 1834 թվականին։ Նա դա արեց՝ վերլուծելով Բոյլ-Մարիոտի, Գեյ-Լյուսակի և Չարլզի գազային օրենքները, որոնք հայտնաբերվեցին 19-րդ դարի սկզբին:
Ռուս քիմիկոս Դմիտրի Մենդելեևի արժանիքը կայանում է նրանում, որ նա հավասարմանը տվել է ժամանակակից և հեշտ օգտագործվող մաթեմատիկական ձև: Մասնավորապես, Մենդելեևը հավասարման մեջ մտցրեց հաստատուն բոլոր գազերի համար R=8, 314 J/(molK): Ինքը՝ Կլապեյրոնը, օգտագործել է մի շարք էմպիրիկ հաստատուններ, որոնք դժվարացնում են հաշվողական գործընթացը։
Մենդելեև-Կլապեյրոն հավասարումը գրված է հետևյալ կերպ.
PV=nRT.
Այս հավասարությունը նշանակում է, որ P ճնշման և V ծավալի արտադրյալը արտահայտության ձախ կողմում միշտ համաչափ է բացարձակ T ջերմաստիճանի արտադրյալին և ձախ կողմում գտնվող n նյութի քանակին:
Ուսումնասիրվող արտահայտությունը թույլ է տալիս ստանալ գազի ցանկացած օրենք, եթե ֆիքսեք դրա չորս պարամետրերից երկուսը: Իզոպրոցեսների դեպքում ուսումնասիրվում են փակ համակարգեր, որոնցում չկա նյութի փոխանակում շրջակա միջավայրի հետ (n=const): Այս գործընթացները բնութագրվում են մեկ ֆիքսված թերմոդինամիկական պարամետրով (T, P կամ V):

Օրինակ խնդիր
Այժմ լուծենք Մենդելեև-Կլապեյրոն հավասարման խնդիրը։ Հայտնի է, որ 500 գրամ կշռող թթվածինը գտնվում է 100 լիտր ծավալով բալոնում՝ 2 մթնոլորտ ճնշման տակ։ Որքա՞ն է օդապարիկի ջերմաստիճանը, հաշվի առնելով, որ համակարգը գտնվում է թերմոդինամիկական հավասարակշռության մեջ։
Հիշեցնենք, որ ըստ սահմանման նյութի քանակությունը հաշվարկվում է բանաձևով՝
n=m/M.
Որտեղ m-ը համակարգի բոլոր մասնիկների զանգվածն է, M-ը նրանց միջին մոլային զանգվածն է: Այս հավասարությունը թույլ է տալիս վերաշարադրել Մենդելեևի հավասարումը հետևյալ ձևով՝
PV=mRT/M.
Որտեղ մենք ստանում ենք այս առաջադրանքի աշխատանքային բանաձևը՝
T=PVM/(mR).
Մնում է բոլոր մեծությունները վերածել SI միավորների և դրանք փոխարինել այս արտահայտությամբ.
T=21013250, 10, 032/(0, 58, 314)=156 Կ.
Հաշվարկված ջերմաստիճանը -117 oC է: Թեև այս ջերմաստիճանում թթվածինը դեռ գազային է (այն խտանում է -182,96 oC), նման պայմաններում իդեալական գազի մոդելը կարող է օգտագործվել միայն հաշվարկված արժեքի որակական գնահատական ստանալու համար:






