Աշխարհը, որտեղ մենք ապրում ենք, աներևակայելի գեղեցիկ է և լի բազմաթիվ տարբեր գործընթացներով, որոնք սահմանում են կյանքի ընթացքը: Այս բոլոր գործընթացներն ուսումնասիրվում են ծանոթ գիտության՝ ֆիզիկայի կողմից։ Այն հնարավորություն է տալիս գոնե որոշակի պատկերացում կազմել տիեզերքի ծագման մասին։ Այս հոդվածում մենք կքննարկենք այնպիսի հասկացություն, ինչպիսին է մոլեկուլային կինետիկ տեսությունը, դրա հավասարումները, տեսակները և բանաձևերը: Այնուամենայնիվ, նախքան այս հարցերի ավելի խորը ուսումնասիրությանը անցնելը, դուք պետք է ինքներդ պարզաբանեք ֆիզիկայի բուն իմաստը և այն ուսումնասիրվող ոլորտները:
Ի՞նչ է ֆիզիկան:

Իրականում սա շատ ծավալուն գիտություն է և, թերևս, մարդկության պատմության մեջ ամենահիմնարարներից մեկը: Օրինակ, եթե նույն համակարգչային գիտությունը կապված է մարդու գործունեության գրեթե բոլոր ոլորտների հետ, լինի դա հաշվողական ձևավորում, թե մուլտֆիլմերի ստեղծում, ապա ֆիզիկան ինքնին կյանք է, նրա բարդ գործընթացների և հոսքերի նկարագրությունը: Փորձենք պարզել դրա իմաստը՝ հնարավորինս պարզեցնելով հասկացողությունը։
ԱյսպեսԱյսպիսով, ֆիզիկան գիտություն է, որը զբաղվում է էներգիայի և նյութի ուսումնասիրությամբ, նրանց միջև կապերով, մեր հսկայական տիեզերքում տեղի ունեցող բազմաթիվ գործընթացների բացատրությամբ: Նյութի կառուցվածքի մոլեկուլային-կինետիկ տեսությունը միայն մի փոքր կաթիլ է ֆիզիկայի տեսությունների և ճյուղերի ծովում:
Էներգիան, որը այս գիտությունը մանրամասն ուսումնասիրում է, կարող է ներկայացվել տարբեր ձևերով: Օրինակ՝ լույսի, շարժման, ձգողականության, ճառագայթման, էլեկտրականության և շատ այլ ձևերի տեսքով։ Այս հոդվածում կանդրադառնանք այս ձևերի կառուցվածքի մոլեկուլային կինետիկ տեսությանը։
Նյութի ուսումնասիրությունը մեզ պատկերացում է տալիս նյութի ատոմային կառուցվածքի մասին: Ի դեպ, դա բխում է մոլեկուլային-կինետիկ տեսությունից. Նյութի կառուցվածքի մասին գիտությունը թույլ է տալիս հասկանալ և գտնել մեր գոյության իմաստը, կյանքի և հենց Տիեզերքի առաջացման պատճառները։ Եկեք դեռ փորձենք ուսումնասիրել նյութի մոլեկուլային կինետիկ տեսությունը:
Նախ, որոշ ներածություն է անհրաժեշտ տերմինաբանությունը և ցանկացած եզրակացություն ամբողջությամբ հասկանալու համար:
Ֆիզիկայի թեմաներ
Պատասխանելով այն հարցին, թե ինչ է մոլեկուլային-կինետիկ տեսությունը, չի կարելի չխոսել ֆիզիկայի բաժինների մասին: Սրանցից յուրաքանչյուրը վերաբերում է մարդու կյանքի որոշակի ոլորտի մանրամասն ուսումնասիրությանը և բացատրությանը: Դրանք դասակարգվում են հետևյալ կերպ՝
- Մեխանիկա, որը բաժանված է ևս երկու բաժնի՝ կինեմատիկա և դինամիկա։
- Ստատիկ.
- Թերմոդինամիկա.
- Մոլեկուլային հատված.
- էլեկտրոդինամիկա.
- Օպտիկա.
- Քվանտների և ատոմային միջուկի ֆիզիկա.
Եկեք կոնկրետ խոսենք մոլեկուլային մասինֆիզիկա, քանի որ այն հիմնված է մոլեկուլային-կինետիկ տեսության վրա։
Ի՞նչ է թերմոդինամիկան:
Ընդհանուր առմամբ, մոլեկուլային մասը և թերմոդինամիկան ֆիզիկայի սերտորեն կապված ճյուղեր են, որոնք ուսումնասիրում են բացառապես ֆիզիկական համակարգերի ընդհանուր թվի մակրոսկոպիկ բաղադրիչը։ Հարկ է հիշել, որ այս գիտությունները ճշգրիտ նկարագրում են մարմինների և նյութերի ներքին վիճակը։ Օրինակ՝ դրանց վիճակը տաքացման, բյուրեղացման, գոլորշիացման և խտացման ժամանակ՝ ատոմային մակարդակում։ Այլ կերպ ասած, մոլեկուլային ֆիզիկան համակարգերի գիտություն է, որը բաղկացած է հսկայական թվով մասնիկներից՝ ատոմներից և մոլեկուլներից:
Հենց այս գիտություններն են ուսումնասիրել մոլեկուլային կինետիկ տեսության հիմնական դրույթները:
Նույնիսկ յոթերորդ դասարանում մենք ծանոթացանք միկրո և մակրոաշխարհներ, համակարգեր հասկացություններին։ Ավելորդ չի լինի թարմացնել այս տերմինները հիշողության մեջ։
Միկրոաշխարհը, ինչպես տեսնում ենք հենց իր անունից, կազմված է տարրական մասնիկներից: Այսինքն՝ սա փոքր մասնիկների աշխարհն է։ Նրանց չափերը չափվում են 10-18 մ-ից մինչև 10-4 մ միջակայքում, և դրանց իրական վիճակի ժամանակը կարող է հասնել և՛ անսահմանության, և՛ անհամաչափ փոքր ընդմիջումներով, օրինակ՝ 10-20 վրկ։
Macroworld-ը դիտարկում է կայուն ձևերի մարմիններ և համակարգեր, որոնք բաղկացած են բազմաթիվ տարրական մասնիկներից: Նման համակարգերը համարժեք են մեր մարդկային չափերին։
Բացի այդ, կա այնպիսի բան, ինչպիսին մեգա աշխարհն է: Այն կազմված է հսկայական մոլորակներից, տիեզերական գալակտիկաներից և բարդույթներից։
Հիմունքներտեսություն
Այժմ, երբ մենք մի փոքր ամփոփեցինք և հիշեցինք ֆիզիկայի հիմնական տերմինները, կարող ենք ուղղակիորեն անցնել այս հոդվածի հիմնական թեմային:
Մոլեկուլային-կինետիկ տեսությունը հայտնվեց և առաջին անգամ ձևակերպվեց XIX դարում: Դրա էությունը կայանում է նրանում, որ այն մանրամասն նկարագրում է ցանկացած նյութի կառուցվածքը (ավելի հաճախ գազերի կառուցվածքը, քան պինդ և հեղուկ մարմինները), հիմնվելով երեք հիմնարար դրույթների վրա, որոնք հավաքվել են այնպիսի նշանավոր գիտնականների ենթադրություններից, ինչպիսիք են Ռոբերտ Հուկը, Իսահակը: Նյուտոնը, Դանիել Բերնուլին, Միխայիլ Լոմոնոսովը և շատ ուրիշներ։
Մոլեկուլային կինետիկ տեսության հիմնական դրույթները հնչում են այսպես.
- Բացարձակապես բոլոր նյութերը (անկախ նրանից՝ հեղուկ են, պինդ, թե գազային) ունեն բարդ կառուցվածք՝ բաղկացած ավելի փոքր մասնիկներից՝ մոլեկուլներից և ատոմներից։ Ատոմները երբեմն կոչվում են «տարրական մոլեկուլներ»:
- Այս բոլոր տարրական մասնիկները միշտ գտնվում են շարունակական և քաոսային շարժման վիճակում։ Մեզանից յուրաքանչյուրը հանդիպել է այս առաջարկի ուղղակի ապացույցին, բայց, ամենայն հավանականությամբ, այն առանձնապես չի կարևորել։ Օրինակ՝ բոլորս էլ տեսանք արեգակի ճառագայթների ֆոնին, որ փոշու մասնիկները անընդհատ շարժվում են քաոսային ուղղությամբ։ Դա պայմանավորված է նրանով, որ ատոմները փոխադարձ հրումներ են առաջացնում միմյանց հետ՝ անընդհատ կինետիկ էներգիա հաղորդելով միմյանց։ Այս երևույթն առաջին անգամ ուսումնասիրվել է 1827 թվականին, և այն անվանվել է հայտնաբերողի անունով՝ «Բրաունյան շարժում»։
- Բոլոր տարրական մասնիկները գտնվում են միմյանց հետ շարունակական փոխազդեցության գործընթացում.որոշակի ուժեր, որոնք ունեն էլեկտրական քար։
Հարկ է նշել, որ թիվ 2 դիրքը նկարագրող մեկ այլ օրինակ, որը նույնպես կարող է կիրառվել, օրինակ, գազերի մոլեկուլային կինետիկ տեսության համար, դիֆուզիան է: Մենք դրան հանդիպում ենք առօրյա կյանքում, ինչպես նաև բազմաթիվ թեստերի և հսկողության ժամանակ, ուստի կարևոր է դրա մասին պատկերացում ունենալ:
Նախ, հաշվի առեք հետևյալ օրինակները.
Բժիշկը պատահաբար սեղանի վրա կոլբայից ալկոհոլ է թափել։ Կամ գուցե դուք գցեցիք ձեր օծանելիքի սրվակը և այն տարածվեց ամբողջ հատակով։
Ինչո՞ւ այս երկու դեպքում և՛ ալկոհոլի, և՛ օծանելիքի հոտը որոշ ժամանակ անց կլցնեն ամբողջ սենյակը, և ոչ միայն այն հատվածը, որտեղ թափվել է այդ նյութերի պարունակությունը:
Պատասխանը պարզ է՝ դիֆուզիոն։
Դիֆուզիա - ինչ է դա: Ինչպե՞ս է այն հոսում:

Սա պրոցես է, երբ մի կոնկրետ նյութ (սովորաբար գազ) կազմող մասնիկները ներթափանցում են մյուսի միջմոլեկուլային դատարկությունները: Վերևի մեր օրինակներում տեղի ունեցավ հետևյալը. ջերմային, այսինքն՝ շարունակական և տարանջատված շարժման պատճառով ալկոհոլի և/կամ օծանելիքի մոլեկուլները ընկան օդի մոլեկուլների միջև ընկած բացերը: Աստիճանաբար, ատոմների և օդի մոլեկուլների հետ բախման ազդեցության տակ, դրանք տարածվում են սենյակում։ Ի դեպ, դիֆուզիայի ինտենսիվությունը, այսինքն՝ դրա հոսքի արագությունը կախված է դիֆուզիոն ներգրավված նյութերի խտությունից, ինչպես նաև դրանց ատոմների և մոլեկուլների շարժման էներգիայից, որը կոչվում է կինետիկ։ Որքան մեծ է կինետիկ էներգիան, այնքան այդ մոլեկուլների համապատասխանաբար բարձր արագությունն ու ինտենսիվությունը։
Ամենաարագ դիֆուզիոն գործընթացը կարելի է անվանել դիֆուզիոն գազերում: Դա պայմանավորված է նրանով, որ գազն իր բաղադրությամբ միատարր չէ, ինչը նշանակում է, որ գազերի միջմոլեկուլային դատարկությունները համապատասխանաբար զգալի տարածություն են զբաղեցնում, և դրանց մեջ օտար նյութի ատոմներ և մոլեկուլներ ներթափանցելու գործընթացը ընթանում է ավելի հեշտ և արագ:.
Հեղուկների մեջ այս գործընթացը մի փոքր ավելի դանդաղ է ընթանում: Շաքարի խորանարդների տարրալուծումը մի գավաթ թեյի մեջ պինդ նյութի հեղուկի մեջ տարածման օրինակ է։
Բայց ամենաերկար ժամանակը դիֆուզիան է ամուր բյուրեղային կառուցվածք ունեցող մարմիններում: Դա հենց այդպես է, քանի որ պինդ մարմինների կառուցվածքը միատարր է և ունի ամուր բյուրեղային ցանց, որի բջիջներում պինդ մարմնի ատոմները թրթռում են։ Օրինակ, եթե երկու մետաղական ձողերի մակերեսները լավ մաքրվեն և հետո շփվեն միմյանց հետ, ապա բավական երկար ժամանակ անց մենք կկարողանանք հայտնաբերել մի մետաղի կտորներ մյուսում և հակառակը։
։
Ինչպես ցանկացած այլ հիմնարար բաժին, ֆիզիկայի հիմնական տեսությունը բաժանված է առանձին մասերի՝ դասակարգում, տեսակներ, բանաձևեր, հավասարումներ և այլն։ Այսպիսով, մենք սովորեցինք մոլեկուլային կինետիկ տեսության հիմունքները: Սա նշանակում է, որ դուք կարող եք ապահով կերպով անցնել առանձին տեսական բլոկների քննարկմանը:
Գազերի մոլեկուլային-կինետիկ տեսություն
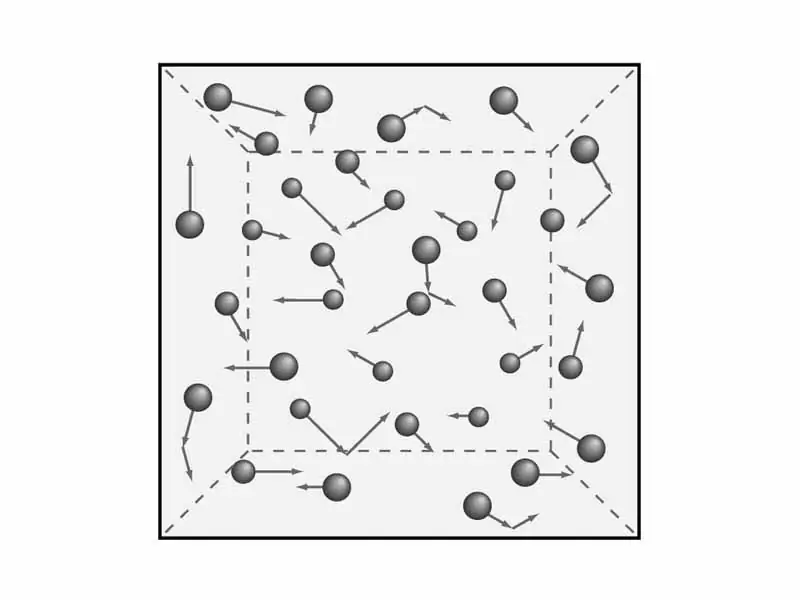
Կա անհրաժեշտություն հասկանալու գազի տեսության դրույթները. Ինչպես արդեն ասացինք, մենք կդիտարկենք գազերի մակրոսկոպիկ բնութագրերը, ինչպիսիք են ճնշումը և ջերմաստիճանը: Սահետագայում անհրաժեշտ կլինի գազերի մոլեկուլային-կինետիկ տեսության հավասարումը ստանալու համար։ Բայց մաթեմատիկան՝ ավելի ուշ, իսկ հիմա եկեք զբաղվենք տեսությամբ և, համապատասխանաբար, ֆիզիկայով։
Գիտնականները ձևակերպել են գազերի մոլեկուլային տեսության հինգ դրույթ, որոնք ծառայում են գազերի կինետիկ մոդելի ըմբռնմանը։ Նրանք հնչում են այսպես.
- Բոլոր գազերը կազմված են տարրական մասնիկներից, որոնք չունեն որոշակի չափ, բայց ունեն որոշակի զանգված։ Այլ կերպ ասած, այս մասնիկների ծավալը նվազագույն է՝ համեմատած նրանց միջև եղած երկարության հետ։
- Գազերի ատոմները և մոլեկուլները գործնականում չունեն պոտենցիալ էներգիա, համապատասխանաբար, ըստ օրենքի, ամբողջ էներգիան հավասար է կինետիկին:
- Այս դիրքին մենք արդեն ծանոթացել ենք ավելի վաղ՝ Բրաունյան շարժում։ Այսինքն՝ գազի մասնիկները միշտ անընդհատ և քաոսային շարժման մեջ են։
- Գազի մասնիկների բացարձակապես բոլոր փոխադարձ բախումները, որոնք ուղեկցվում են արագության և էներգիայի հաղորդագրությամբ, լիովին առաձգական են։ Սա նշանակում է, որ բախման ժամանակ էներգիայի կորուստ կամ կտրուկ թռիչք չկա նրանց կինետիկ էներգիայի մեջ։
- Նորմալ պայմաններում և հաստատուն ջերմաստիճանում գրեթե բոլոր գազերի մասնիկների շարժման միջին էներգիան նույնն է։
Գազերի մոլեկուլային-կինետիկ տեսության այս տեսակի հավասարման միջոցով մենք կարող ենք վերաշարադրել հինգերորդ դիրքը.
E=1/2mv^2=3/2kT, որտեղ k-ը Բոլցմանի հաստատունն է; T - ջերմաստիճանը Կելվինում:
Այս հավասարումը մեզ ստիպում է հասկանալ գազի տարրական մասնիկների արագության և դրանց բացարձակ ջերմաստիճանի միջև կապը: Ըստ այդմ, որքան բարձր է նրանց բացարձակըջերմաստիճանը, այնքան մեծ է նրանց արագությունը և կինետիկ էներգիան։
Գազի ճնշում
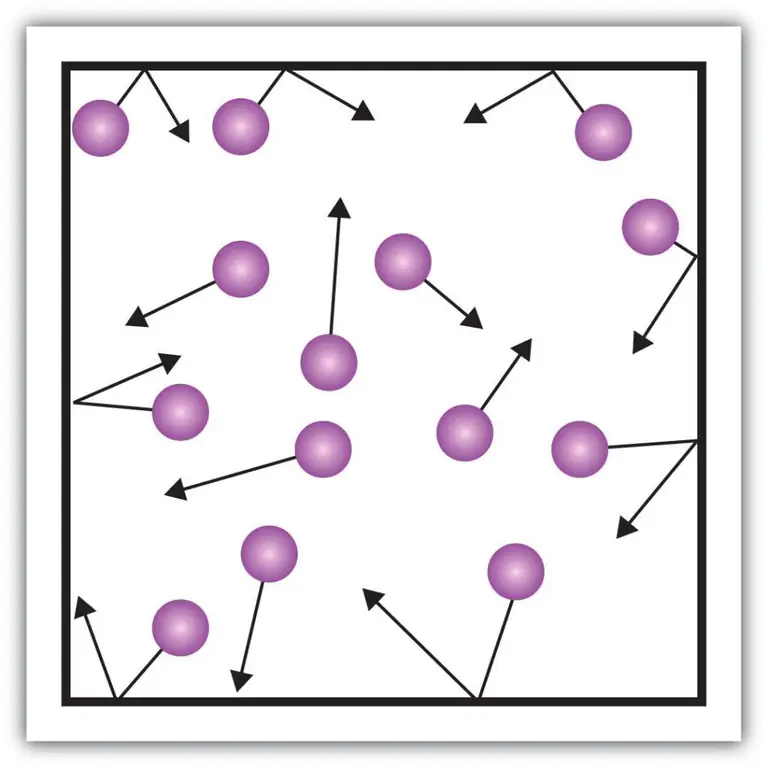
Բնութագրի այնպիսի մակրոսկոպիկ բաղադրիչները, ինչպիսիք են գազերի ճնշումը, կարող են բացատրվել նաև կինետիկ տեսության միջոցով: Դա անելու համար եկեք պատկերացնենք հետևյալ օրինակը։
Ենթադրենք, որ որոշ գազի մոլեկուլ գտնվում է տուփի մեջ, որի երկարությունը L է: Եկեք օգտագործենք վերը նկարագրված գազի տեսության դրույթները և հաշվի առնենք այն փաստը, որ մոլեկուլային գունդը շարժվում է միայն x-ի երկայնքով: - առանցք. Այսպիսով, մենք կկարողանանք դիտարկել նավի պատերից մեկի հետ առաձգական բախման գործընթացը (տուփ):
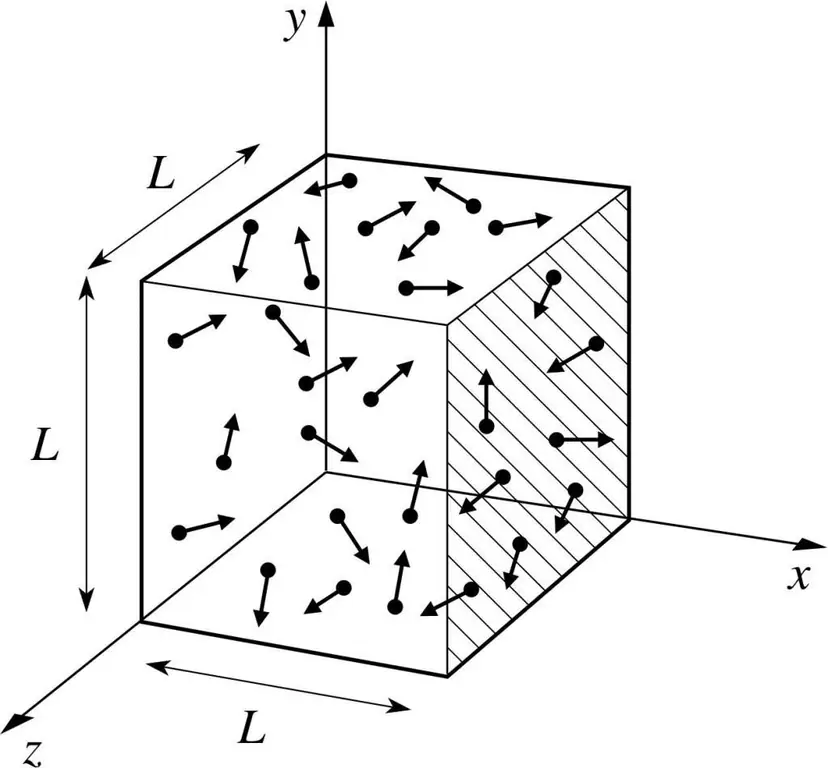
Ընթացիկ բախման իմպուլսը, ինչպես գիտենք, որոշվում է p=mv բանաձևով, բայց այս դեպքում այս բանաձևը կստանա պրոյեկցիոն ձև՝ p=mv(x).
Քանի որ մենք դիտարկում ենք միայն x առանցքի չափը, այսինքն՝ x առանցքը, իմպուլսի ընդհանուր փոփոխությունը կարտահայտվի բանաձևով՝ mv(x) - m(-v(x))=2mv(x).
Հաջորդ, դիտարկենք մեր օբյեկտի գործադրած ուժը՝ օգտագործելով Նյուտոնի երկրորդ օրենքը՝ F=ma=P/t։
Այս բանաձևերից մենք արտահայտում ենք ճնշումը գազի կողմից՝ P=F/a;
Այժմ եկեք փոխարինենք ուժի արտահայտությունը ստացված բանաձևով և ստացվի՝ P=mv(x)^2/L^3.
Դրանից հետո մեր ավարտված ճնշման բանաձևը կարելի է գրել գազի մոլեկուլների N-րդ թվի համար: Այլ կերպ ասած, այն կունենա հետևյալ տեսքը՝
P=Nmv(x)^2/V, որտեղ v-ն արագությունն է, իսկ V-ը՝ ծավալը։
Այժմ փորձենք առանձնացնել գազի ճնշման վերաբերյալ մի քանի հիմնական դրույթներ.
- Դա դրսևորվում է միջոցովմոլեկուլների բախումներ այն օբյեկտի պատերի մոլեկուլների հետ, որոնցում այն գտնվում է։
- Ճնշման մեծությունն ուղիղ համեմատական է նավի պատերի վրա մոլեկուլների ազդեցության ուժին և արագությանը։
Որոշ հակիրճ եզրակացություններ տեսության վերաբերյալ
Նախքան ավելի հեռուն գնալը և մոլեկուլային կինետիկ տեսության հիմնական հավասարումը դիտարկելը, մենք ձեզ առաջարկում ենք մի քանի հակիրճ եզրակացություն վերը նշված կետերից և տեսությունից.
- Նրա ատոմների և մոլեկուլների շարժման միջին էներգիայի չափումը բացարձակ ջերմաստիճանն է։
- Երբ երկու տարբեր գազեր գտնվում են նույն ջերմաստիճանում, նրանց մոլեկուլներն ունեն նույն միջին կինետիկ էներգիան։
- Գազի մասնիկների էներգիան ուղիղ համեմատական է միջին քառակուսի արագությանը. E=1/2mv^2.
- Չնայած գազի մոլեկուլներն ունեն համապատասխանաբար միջին կինետիկ էներգիա և միջին արագություն, առանձին մասնիկներ շարժվում են տարբեր արագություններով՝ ոմանք արագ, ոմանք՝ դանդաղ։
- Որքան բարձր է ջերմաստիճանը, այնքան բարձր է մոլեկուլների արագությունը:
- Քանի՞ անգամ ենք բարձրացնում գազի ջերմաստիճանը (օրինակ՝ կրկնակի), նրա մասնիկների շարժման էներգիան ավելանում է նույնքան անգամ (համապատասխանաբար՝ կրկնապատկվում):
Հիմնական հավասարում և բանաձևեր

Մոլեկուլային կինետիկ տեսության հիմնական հավասարումը թույլ է տալիս կապ հաստատել միկրոաշխարհի մեծությունների և, համապատասխանաբար, մակրոսկոպիկ, այսինքն՝ չափված մեծությունների միջև։
Ամենապարզ մոդելներից մեկը, որը կարող է դիտարկել մոլեկուլային տեսությունը, իդեալական գազի մոդելն է:
Կարելի է դա ասելսա իդեալական գազի մոլեկուլային կինետիկ տեսության կողմից ուսումնասիրված երևակայական մոդել է, որտեղ՝
- ամենապարզ գազի մասնիկները համարվում են կատարյալ առաձգական գնդիկներ, որոնք փոխազդում են և՛ միմյանց, և՛ ցանկացած նավի պատերի մոլեկուլների հետ միայն մեկ դեպքում՝ բացարձակ առաձգական բախում;
- Գազի ներսում ձգող ուժերը բացակայում են, կամ դրանք կարող են իրականում անտեսվել;
- տարրերը, այսինքն՝ դրանց ծավալը նույնպես կարելի է անտեսել։
Որպես նյութական կետեր կարելի է ընդունել գազի ներքին կառուցվածքի
Հաշվի առնելով նման մոդելը՝ գերմանացի ֆիզիկոս Ռուդոլֆ Կլաուզիուսը գրել է գազի ճնշման բանաձև՝ միկրո և մակրոսկոպիկ պարամետրերի փոխհարաբերությունների միջոցով: Կարծես՝
p=1/3m(0)nv^2.
Հետագայում այս բանաձևը կկոչվի որպես իդեալական գազի մոլեկուլային-կինետիկ տեսության հիմնական հավասարում: Այն կարող է ներկայացվել մի քանի տարբեր ձևերով. Այժմ մեր պարտականությունն է ցույց տալ այնպիսի բաժիններ, ինչպիսիք են մոլեկուլային ֆիզիկան, մոլեկուլային կինետիկ տեսությունը և, հետևաբար, դրանց ամբողջական հավասարումները և տեսակները: Հետևաբար, իմաստ ունի դիտարկել հիմնական բանաձևի այլ տարբերակներ:
Մենք գիտենք, որ գազի մոլեկուլների շարժումը բնութագրող միջին էներգիան կարելի է գտնել՝ օգտագործելով բանաձևը՝ E=m(0)v^2/2:
Այս դեպքում մենք կարող ենք սկզբնական ճնշման բանաձևում m(0)v^2 արտահայտությունը փոխարինել միջին կինետիկ էներգիայով: Սրա արդյունքում մենք հնարավորություն կունենանք կազմելու գազերի մոլեկուլային կինետիկ տեսության հիմնական հավասարումը հետևյալ ձևով՝ p=2/3nE.
Բացի այդ, մենք բոլորս գիտենք, որ m(0)n արտահայտությունը կարելի է գրել որպես երկու գործակիցների արտադրյալ.
m/NN/V=m/V=ρ.
Այս մանիպուլյացիաներից հետո մենք կարող ենք վերաշարադրել մեր բանաձևը իդեալական գազի մոլեկուլային-կինետիկ տեսության հավասարման երրորդ, տարբեր ձևով.
p=1/3ρv^2.
Դե, գուցե դա այն ամենն է, ինչ դուք պետք է իմանաք այս թեմայով: Մնում է միայն համակարգել ձեռք բերված գիտելիքները հակիրճ (և ոչ այնքան) եզրակացությունների տեսքով։
Բոլոր ընդհանուր եզրակացությունները և բանաձևերը «Մոլեկուլյար-կինետիկ տեսություն» թեմայով
Ուրեմն եկեք սկսենք:
Առաջին:
Ֆիզիկան բնագիտության կուրսում ընդգրկված հիմնարար գիտություն է, որն ուսումնասիրում է նյութի և էներգիայի հատկությունները, դրանց կառուցվածքը, անօրգանական բնույթի օրինաչափությունները։
Այն ներառում է հետևյալ բաժինները.
- մեխանիկա (կինեմատիկա և դինամիկա);
- ստատիկ;
- թերմոդինամիկա;
- էլեկտրոդինամիկա;
- մոլեկուլային հատված;
- օպտիկա;
- քվանտների և ատոմային միջուկի ֆիզիկա.
Երկրորդ՝
Մասնիկների ֆիզիկան և թերմոդինամիկան սերտորեն փոխկապակցված ճյուղեր են, որոնք ուսումնասիրում են ֆիզիկական համակարգերի ընդհանուր թվի բացառապես մակրոսկոպիկ բաղադրիչը, այսինքն՝ համակարգերը, որոնք բաղկացած են հսկայական թվով տարրական մասնիկներից:
Դրանք հիմնված են մոլեկուլային կինետիկ տեսության վրա։
Երրորդ:
Խնդիրի էությունը սա է. Մոլեկուլային կինետիկ տեսությունը մանրամասն նկարագրում է նյութի կառուցվածքը (ավելի հաճախ գազերի կառուցվածքը, քան պինդ մարմինները)։և հեղուկ մարմիններ), հիմնված երեք հիմնարար ենթադրությունների վրա, որոնք հավաքվել են նշանավոր գիտնականների ենթադրություններից։ Նրանց թվում են՝ Ռոբերտ Հուկը, Իսահակ Նյուտոնը, Դանիել Բերնուլին, Միխայիլ Լոմոնոսովը և շատ ուրիշներ։
Չորրորդ:
Մոլեկուլային կինետիկ տեսության երեք հիմնական դրույթներ.
- Բոլոր նյութերը (անկախ նրանից, թե դրանք հեղուկ են, պինդ կամ գազային) ունեն բարդ կառուցվածք, որը բաղկացած է փոքր մասնիկներից՝ մոլեկուլներից և ատոմներից:
- Այս բոլոր պարզ մասնիկները գտնվում են շարունակական քաոսային շարժման մեջ: Օրինակ՝ Բրոունյան շարժում և դիֆուզիա։
- Բոլոր մոլեկուլները ցանկացած պայմաններում փոխազդում են միմյանց հետ որոշակի ուժերով, որոնք ունեն էլեկտրական քար:
Մոլեկուլային կինետիկ տեսության այս դրույթներից յուրաքանչյուրը ամուր հիմք է նյութի կառուցվածքի ուսումնասիրության համար:
Հինգերորդ:
Մոլեկուլային տեսության մի քանի հիմնական կետեր գազի մոդելի համար.
- Բոլոր գազերը կազմված են տարրական մասնիկներից, որոնք չունեն որոշակի չափ, բայց ունեն որոշակի զանգված։ Այլ կերպ ասած, այս մասնիկների ծավալը նվազագույն է նրանց միջև եղած հեռավորությունների համեմատ։
- Գազերի ատոմները և մոլեկուլները գործնականում չունեն պոտենցիալ էներգիա, համապատասխանաբար նրանց ընդհանուր էներգիան հավասար է կինետիկին։
- Այս դիրքին մենք արդեն ծանոթացել ենք ավելի վաղ՝ Բրաունյան շարժում։ Այսինքն՝ գազի մասնիկները միշտ անընդհատ և պատահական շարժման մեջ են։
- Ատոմների և գազերի մոլեկուլների բացարձակապես բոլոր փոխադարձ բախումները, որոնք ուղեկցվում են արագության և էներգիայի հաղորդագրությամբ, լիովին առաձգական են: Սանշանակում է, որ բախման ժամանակ էներգիայի կորուստ կամ կտրուկ թռիչք չկա նրանց կինետիկ էներգիայի մեջ։
- Նորմալ պայմաններում և հաստատուն ջերմաստիճանում գրեթե բոլոր գազերի միջին կինետիկ էներգիան նույնն է։
Վեցերորդ:
Եզրակացություններ գազերի մասին տեսությունից.
- Բացարձակ ջերմաստիճանը նրա ատոմների և մոլեկուլների միջին կինետիկ էներգիայի չափումն է։
- Երբ երկու տարբեր գազեր գտնվում են նույն ջերմաստիճանում, նրանց մոլեկուլներն ունեն նույն միջին կինետիկ էներգիան։
- Գազի մասնիկների միջին կինետիկ էներգիան ուղիղ համեմատական է արմատի միջին քառակուսի արագությանը. E=1/2mv^2։
- Չնայած գազի մոլեկուլներն ունեն համապատասխանաբար միջին կինետիկ էներգիա և միջին արագություն, առանձին մասնիկներ շարժվում են տարբեր արագություններով՝ ոմանք արագ, ոմանք՝ դանդաղ։
- Որքան բարձր է ջերմաստիճանը, այնքան բարձր է մոլեկուլների արագությունը:
- Քանի՞ անգամ ենք բարձրացնում գազի ջերմաստիճանը (օրինակ՝ կրկնակի), այդքան անգամ ավելանում է նաև նրա մասնիկների միջին կինետիկ էներգիան (համապատասխանաբար՝ կրկնապատկվում):
- Գազի ճնշման կապը անոթի պատերի վրա, որտեղ այն գտնվում է, և մոլեկուլների ներգործության ինտենսիվությունը այդ պատերին ուղիղ համեմատական է. որքան շատ հարվածներ, այնքան բարձր ճնշումը և հակառակը.
Յոթերորդ:
Իդեալական գազի մոդելը այն մոդելն է, որի դեպքում պետք է բավարարվեն հետևյալ պայմանները.
- Գազի մոլեկուլները կարող են և համարվում են կատարյալ առաձգական գնդիկներ:
- Այս գնդակները կարող են փոխազդել միմյանց և ցանկացածի պատերի հետանոթ միայն մեկ դեպքում՝ բացարձակ առաձգական բախում։
- Այն ուժերը, որոնք նկարագրում են գազի ատոմների և մոլեկուլների միջև փոխադարձ մղումը, բացակայում են կամ կարող են իրականում անտեսվել:
- Ատոմներն ու մոլեկուլները համարվում են նյութական կետեր, այսինքն՝ դրանց ծավալը նույնպես կարելի է անտեսել։
Ութերորդ:
Տրենք բոլոր հիմնական հավասարումները և ցույց տանք «Մոլեկուլյար-կինետիկ տեսություն» թեմայի բանաձևերը:
p=1/3m(0)nv^2 - իդեալական գազի մոդելի հիմնական հավասարումը, որը ստացվել է գերմանացի ֆիզիկոս Ռուդոլֆ Կլաուզիուսի կողմից:
p=2/3nE - իդեալական գազի մոլեկուլային-կինետիկ տեսության հիմնական հավասարումը։ Ստացվում է մոլեկուլների միջին կինետիկ էներգիայից։
р=1/3ρv^2 - նույն հավասարումը, բայց դիտարկվում է իդեալական գազի մոլեկուլների խտության և արմատի միջին քառակուսի արագության միջոցով:
m(0)=M/N(a) - Ավոգադրոյի թվով մեկ մոլեկուլի զանգվածը գտնելու բանաձև։
v^2=(v(1)+v(2)+v(3)+…)/N - մոլեկուլների միջին քառակուսի արագությունը գտնելու բանաձև, որտեղ v(1), v(2), v (3) և այլն - առաջին մոլեկուլի արագությունը, երկրորդը, երրորդը և այլն մինչև n-րդ մոլեկուլը։
n=N/V - մոլեկուլների կոնցենտրացիան գտնելու բանաձև, որտեղ N-ը գազի ծավալի մոլեկուլների թիվն է մինչև տվյալ ծավալը V:
E=mv^2/2=3/2kT - մոլեկուլների միջին կինետիկ էներգիան գտնելու բանաձևեր, որտեղ v^2-ը մոլեկուլների միջին քառակուսի արագությունն է, k-ն հաստատուն է արժեքը անվանվել է ավստրիացի Լյուդվիգ Բոլցմանի ֆիզիկայի պատվին, իսկ T-ն գազի ջերմաստիճանն է։
p=nkT - ճնշման բանաձեւը կոնցենտրացիայի առումով, հաստատունԲոլցմանը և բացարձակ ջերմաստիճանը: Դրանից բխում է մեկ այլ հիմնարար բանաձև, որը հայտնաբերել են ռուս գիտնական Մենդելեևը և ֆրանսիացի ֆիզիկոս-ինժեներ Կլայպերոնը.
pV=m/MRT, որտեղ R=kN(a) գազերի համընդհանուր հաստատունն է։
Այժմ եկեք ցույց տանք հաստատուններ տարբեր իզո գործընթացների համար՝ իզոբար, իզոխորիկ, իզոթերմային և ադիաբատիկ:
pV/T=const - կատարվում է, երբ գազի զանգվածը և բաղադրությունը հաստատուն են:
рV=const - եթե ջերմաստիճանը նույնպես հաստատուն է։
V/T=const - եթե գազի ճնշումը հաստատուն է:
p/T=const - եթե ծավալը հաստատուն է:
Հավանաբար դա այն ամենն է, ինչ դուք պետք է իմանաք այս թեմայով:
Այսօր մենք ընկանք այնպիսի գիտական դաշտ, ինչպիսին է տեսական ֆիզիկան, նրա բազմաթիվ բաժիններն ու բլոկները: Ավելի մանրամասն, մենք անդրադարձանք ֆիզիկայի այնպիսի ոլորտին, ինչպիսիք են հիմնարար մոլեկուլային ֆիզիկան և թերմոդինամիկան, մասնավորապես, մոլեկուլային-կինետիկ տեսությունը, որը, կարծես թե, որևէ դժվարություն չի ներկայացնում նախնական ուսումնասիրության մեջ, բայց իրականում ունի բազմաթիվ թակարդներ:. Այն ընդլայնում է մեր պատկերացումները գազի իդեալական մոդելի մասին, որը մենք նույնպես մանրամասն ուսումնասիրել ենք: Բացի այդ, հարկ է նշել, որ մենք նաև ծանոթացանք մոլեկուլային տեսության հիմնական հավասարումների հետ դրանց տարբեր տատանումներով, ինչպես նաև դիտարկեցինք այս թեմայի վերաբերյալ որոշակի անհայտ մեծություններ գտնելու բոլոր ամենաանհրաժեշտ բանաձևերը: Սա հատկապես օգտակար կլինի գրելու պատրաստման ժամանակ: ցանկացած թեստեր, քննություններ և թեստեր, կամ ընդլայնել ֆիզիկայի ընդհանուր տեսակետն ու գիտելիքները:
Հուսով ենք, որ այս հոդվածը օգտակար էր ձեզ համար, և դուք դրանից քաղել եք միայն ամենաանհրաժեշտ տեղեկատվությունը, ամրապնդելով ձեր գիտելիքները թերմոդինամիկայի այնպիսի սյուների վերաբերյալ, ինչպիսիք են մոլեկուլային կինետիկ տեսության հիմնական դրույթները:






