Հեղուկ ջրի եռաչափ վիճակը դժվար է ուսումնասիրել, սակայն շատ բան է սովորել՝ վերլուծելով սառցե բյուրեղների կառուցվածքը: Չորս հարեւան ջրածնի հետ փոխազդող թթվածնի ատոմները զբաղեցնում են քառաեդրոնի գագաթները (տետրա=չորս, հեդրոն=հարթություն)։ Սառույցում նման կապը կոտրելու համար պահանջվող միջին էներգիան գնահատվում է 23 կՋ/մոլ-1:

Ջրի մոլեկուլների՝ որոշակի քանակությամբ ջրածնային շղթաներ ձևավորելու ունակությունը, ինչպես նաև տվյալ ուժը, ստեղծում են անսովոր բարձր հալման կետ: Երբ այն հալվում է, այն պահում է հեղուկ ջրով, որի կառուցվածքն անկանոն է։ Ջրածնային կապերի մեծ մասը աղավաղված է։ Ջրածնային կապակցված սառույցի բյուրեղային ցանցը կոտրելու համար ջերմության տեսքով մեծ քանակությամբ էներգիա է պահանջվում։
Սառույցի տեսքի առանձնահատկությունները (Ih)
Բնակիչներից շատերին հետաքրքրում է, թե ինչպիսի բյուրեղյա վանդակավոր սառույց կա: Անհրաժեշտ էՀարկ է նշել, որ նյութերի մեծ մասի խտությունը մեծանում է սառեցման ժամանակ, երբ մոլեկուլային շարժումները դանդաղում են և առաջանում են խիտ փաթեթավորված բյուրեղներ։ Ջրի խտությունը նույնպես մեծանում է, երբ այն սառչում է առավելագույնը 4°C (277K): Այնուհետև, երբ ջերմաստիճանը իջնում է այս արժեքից ցածր, այն ընդլայնվում է։
Այս աճը պայմանավորված է բաց, ջրածնային կապով սառցե բյուրեղի ձևավորմամբ՝ իր վանդակավոր և ավելի ցածր խտությամբ, որտեղ յուրաքանչյուր ջրի մոլեկուլ կոշտ կապված է վերը նշված տարրով և չորս այլ արժեքներով՝ միաժամանակ բավական արագ շարժվելով։ ավելի մեծ զանգված ունեն: Քանի որ այս գործողությունը տեղի է ունենում, հեղուկը սառչում է վերևից ներքև: Սա կարևոր կենսաբանական արդյունքներ է ունենում, ինչի արդյունքում լճակի սառույցի շերտը կենդանի էակներին մեկուսացնում է ծայրահեղ ցրտից։ Բացի այդ, ջրի երկու լրացուցիչ հատկություն կապված է նրա ջրածնի բնութագրերի հետ՝ հատուկ ջերմություն և գոլորշիացում:
Կառուցվածքների մանրամասն նկարագրություն
Առաջին չափանիշը նյութի 1 գրամ ջերմաստիճանը 1°C-ով բարձրացնելու համար անհրաժեշտ քանակությունն է: Ջրի աստիճանների բարձրացումը պահանջում է համեմատաբար մեծ քանակությամբ ջերմություն, քանի որ յուրաքանչյուր մոլեկուլ ներգրավված է բազմաթիվ ջրածնային կապերի մեջ, որոնք պետք է կոտրվեն, որպեսզի կինետիկ էներգիան մեծանա: Ի դեպ, բոլոր խոշոր բազմաբջիջ օրգանիզմների բջիջներում և հյուսվածքներում H2O-ի առատությունը նշանակում է, որ բջիջների ներսում ջերմաստիճանի տատանումները նվազագույնի են հասցվում։ Այս հատկանիշը կարևոր է, քանի որ կենսաքիմիական ռեակցիաների մեծ մասի արագությունըզգայուն։
Ջրի գոլորշիացման ջերմությունը նույնպես զգալիորեն ավելի բարձր է, քան շատ այլ հեղուկների ջերմությունը: Այս մարմինը գազի վերածելու համար պահանջվում է մեծ քանակությամբ ջերմություն, քանի որ ջրածնային կապերը պետք է կոտրվեն, որպեսզի ջրի մոլեկուլները տեղահանվեն միմյանցից և մտնեն նշված փուլ։ Փոփոխվող մարմինները մշտական դիպոլներ են և կարող են փոխազդել այլ նմանատիպ միացությունների և նրանց հետ, որոնք իոնացվում և լուծվում են:
Մյուս վերը նշված նյութերը կարող են շփվել միայն բևեռականության առկայության դեպքում: Հենց այս միացությունն է ներգրավված այս տարրերի կառուցվածքում: Բացի այդ, այն կարող է հարթեցնել էլեկտրոլիտներից ձևավորված այս մասնիկների շուրջ, այնպես որ ջրի մոլեկուլների թթվածնի բացասական ատոմները կողմնորոշվեն դեպի կատիոնները, իսկ դրական իոնները և ջրածնի ատոմները՝ դեպի անիոնները։
Պինդ մարմիններում, որպես կանոն, առաջանում են մոլեկուլային բյուրեղային ցանցեր և ատոմային ցանցեր։ Այսինքն, եթե յոդը կառուցված է այնպես, որ պարունակում է I2, , ապա պինդ ածխաթթու գազում, այսինքն՝ չոր սառույցի մեջ, CO2 մոլեկուլներ են. տեղակայված բյուրեղային ցանցի հանգույցներում: Նմանատիպ նյութերի հետ փոխազդեցության ժամանակ սառույցն ունի իոնային բյուրեղյա վանդակ: Գրաֆիտը, օրինակ, որն ունի ածխածնի վրա հիմնված ատոմային կառուցվածք, ի վիճակի չէ փոխել այն, ինչպես ադամանդը։
Ինչ է տեղի ունենում, երբ կերակրի աղի բյուրեղը լուծվում է ջրի մեջ. բևեռային մոլեկուլները ձգվում են բյուրեղի լիցքավորված տարրերով, ինչը հանգեցնում է նրա մակերեսի վրա նատրիումի և քլորիդի նմանատիպ մասնիկների առաջացմանը, ինչի արդյունքում առաջանում են այդ մարմինները:տեղահանվում են միմյանցից, և այն սկսում է լուծարվել: Այստեղից կարելի է նկատել, որ սառույցն ունի բյուրեղյա վանդակ՝ իոնային կապով։ Յուրաքանչյուր լուծված Na + ձգում է մի քանի ջրի մոլեկուլների բացասական ծայրերը, մինչդեռ յուրաքանչյուր լուծարված Cl-ը գրավում է դրական ծայրերը: Յուրաքանչյուր իոն շրջապատող թաղանթը կոչվում է փախուստի գունդ և սովորաբար պարունակում է լուծիչի մասնիկների մի քանի շերտեր:
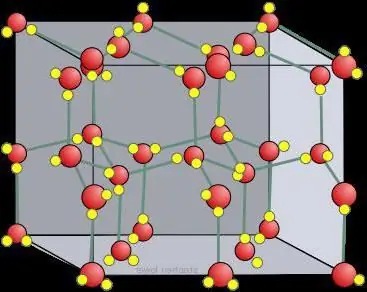
Չոր սառույցի բյուրեղյա վանդակ
Փոփոխականները կամ տարրերով շրջապատված իոնները համարվում են սուլֆատացված: Երբ լուծիչը ջուր է, այդպիսի մասնիկները ջրվում են։ Այսպիսով, ցանկացած բևեռային մոլեկուլ հակված է լուծվել հեղուկ մարմնի տարրերով: Չոր սառույցի մեջ բյուրեղային ցանցի տեսակը ագրեգացման վիճակում առաջացնում է ատոմային կապեր, որոնք անփոփոխ են։ Մեկ այլ բան է բյուրեղային սառույցը (սառեցված ջուր): Իոնային օրգանական միացությունները, ինչպիսիք են կարբոքսիլազը և պրոտոնացված ամինները, պետք է լուծելի լինեն հիդրօքսիլ և կարբոնիլ խմբերում: Նման կառույցներում պարունակվող մասնիկները շարժվում են մոլեկուլների միջև, և դրանց բևեռային համակարգերը ջրածնային կապեր են կազմում այս մարմնի հետ։
Իհարկե, մոլեկուլի վերջին նշված խմբերի քանակը ազդում է դրա լուծելիության վրա, ինչը նույնպես կախված է տարրի տարբեր կառուցվածքների ռեակցիայից. օրինակ՝ մեկ, երկու և երեք ածխածնային սպիրտները խառնվում են։ ջրով, սակայն մեկ հիդրօքսիլային միացություններով ավելի մեծ ածխաջրածինները շատ ավելի քիչ են նոսրանում հեղուկներում։
Վեցանկյուն Ih-ն իր ձևով նման էատոմային բյուրեղյա վանդակ. Սառույցի և ամբողջ բնական ձյան համար Երկրի վրա այն հենց այսպիսի տեսք ունի. Դրա մասին է վկայում ջրի գոլորշիներից (այսինքն՝ ձյան փաթիլներից) աճեցված սառույցի բյուրեղային ցանցի համաչափությունը։ Այն գտնվում է տիեզերական P խմբում 63/մմ 194-ից; D 6h, Laue դաս 6 / մմ; նման է β-ին, որն ունի 6 պարուրաձև առանցքի բազմապատիկ (պտույտ շուրջը, բացի դրա երկայնքով տեղաշարժվելուց): Այն ունի բավականին բաց ցածր խտության կառուցվածք, որտեղ արդյունավետությունը ցածր է (~1/3)՝ համեմատած պարզ խորանարդ (~1/2) կամ դեմքի կենտրոնացված խորանարդ (~3/4) կառուցվածքների հետ:
Համեմատած սովորական սառույցի հետ՝ չոր սառույցի բյուրեղային ցանցը, որը կապված է CO2 մոլեկուլներով, ստատիկ է և փոխվում է միայն այն ժամանակ, երբ ատոմները քայքայվում են:
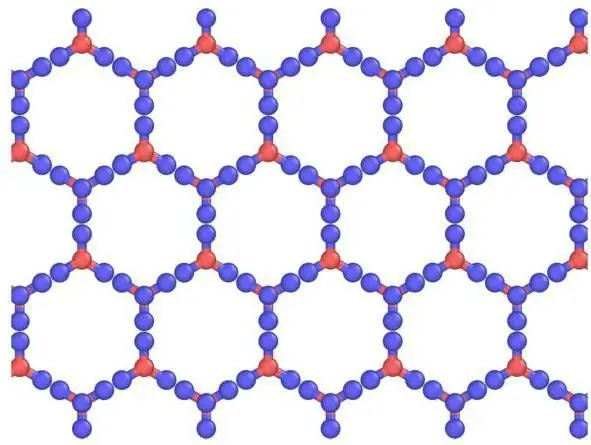
Վանդակաճաղերի և դրանց տարրերի նկարագրությունը
Բյուրեղները կարելի է դիտել որպես բյուրեղային մոդելներ, որոնք բաղկացած են թերթերից, որոնք տեղադրված են մեկը մյուսի վերևում: Ջրածնային կապը դասավորված է, մինչդեռ իրականում այն պատահական է, քանի որ պրոտոնները կարող են շարժվել ջրի (սառույցի) մոլեկուլների միջև մոտ 5 Կ-ից բարձր ջերմաստիճանի դեպքում: Իրոք, հավանական է, որ պրոտոններն իրենց պահեն ինչպես քվանտային հեղուկ՝ մշտական թունելային հոսքում: Սա ուժեղանում է նեյտրոնների ցրման արդյունքում՝ ցույց տալով նրանց ցրման խտությունը թթվածնի ատոմների միջև կիսով չափ՝ ցույց տալով տեղայնացումը և համաձայնեցված շարժումը։ Այստեղ կա սառույցի նմանություն ատոմային, մոլեկուլային բյուրեղային ցանցի հետ:
Մոլեկուլներն ունեն ջրածնի շղթայի աստիճանական դասավորվածությունինքնաթիռում գտնվող իր երեք հարեւանների նկատմամբ։ Չորրորդ տարրն ունի խավարած ջրածնային կապի դասավորություն։ Կատարյալ վեցանկյուն համաչափությունից մի փոքր շեղում կա, քանի որ միավորի բջիջն այս շղթայի ուղղությամբ 0,3%-ով ավելի կարճ է: Բոլոր մոլեկուլները զգում են նույն մոլեկուլային միջավայրերը: Յուրաքանչյուր «տուփի» ներսում բավականաչափ տարածություն կա միջքաղաքային ջրի մասնիկները պահելու համար: Թեև դրանք ընդհանուր առմամբ դիտարկված չեն, դրանք վերջերս արդյունավետորեն հայտնաբերվել են սառույցի փոշի բյուրեղային ցանցի նեյտրոնային դիֆրակցիայի միջոցով:
Փոփոխվող նյութեր
Վեցանկյուն մարմինն ունի եռակի կետ՝ հեղուկ և գազային ջրով 0,01°C, 612 Պա, պինդ տարրեր՝ երեք -21,985°C, 209,9 ՄՊա, տասնմեկ և երկու -199,8°C, 70 ՄՊա, ինչպես նաև. 34,7 ° C, 212,9 ՄՊա: Վեցանկյուն սառույցի դիէլեկտրական հաստատունը 97,5 է։
Այս տարրի հալման կորը տրված է MPa-ով: Վիճակի հավասարումները, բացի դրանցից, հասանելի են որոշ պարզ անհավասարություններ, որոնք կապված են ֆիզիկական հատկությունների փոփոխությունը վեցանկյուն սառույցի և նրա ջրային կախույթների ջերմաստիճանի հետ: Կարծրությունը տատանվում է գիպսից (≦2) կամ ցածր աստիճանի բարձրացումով 0°C-ում մինչև դաշտային սպաթ (6 Mohs) -80°C-ում, բացարձակ կարծրության աննորմալ մեծ փոփոխություն (> 24 անգամ):
Սառույցի վեցանկյուն բյուրեղյա վանդակը ձևավորում է վեցանկյուն թիթեղներ և սյուներ, որտեղ վերին և ստորին երեսները հիմքային հարթություններն են {0 0 0 1} 5,57 մՋ սմ էնթալպիայով -2, և մյուս համարժեք կողային մասերը կոչվում են պրիզմայի մասեր {1 0 -1 0} 5, 94-ով:μJ սմ -2: Երկրորդական մակերեսներ {1 1 -2 0} 6,90 ՄՋ ˣ սմ -2 կարող են ձևավորվել կառույցների կողքերից ձևավորված հարթությունների երկայնքով։
Նման կառուցվածքը ցույց է տալիս ջերմային հաղորդունակության անոմալ նվազում ճնշման աճով (ինչպես նաև ցածր խտության խորանարդ և ամորֆ սառույց), սակայն տարբերվում է բյուրեղներից շատերից։ Դա պայմանավորված է ջրածնային կապի փոփոխությամբ, որը նվազեցնում է ձայնի լայնակի արագությունը սառույցի և ջրի բյուրեղային ցանցում:
Կան մեթոդներ, որոնք նկարագրում են, թե ինչպես պատրաստել մեծ բյուրեղյա նմուշներ և ցանկացած ցանկալի սառցե մակերես: Ենթադրվում է, որ ուսումնասիրվող վեցանկյուն մարմնի մակերեսի ջրածնային կապը ավելի կարգավորված կլինի, քան զանգվածային համակարգի ներսում: Տարբերակային սպեկտրոսկոպիան փուլային ցանցային հաճախականության գեներացմամբ ցույց է տվել, որ վեցանկյուն սառույցի բազալ մակերեսի ստորգետնյա HO շղթայում կա կառուցվածքային անհամաչափություն երկու վերին շերտերի (L1 և L2) միջև: Ընդունված ջրածնային կապերը վեցանկյունների վերին շերտերում (L1 O ··· HO L2) ավելի ամուր են, քան երկրորդ շերտում ընդունվածները դեպի վերին կուտակում (L1 OH ··· O L2): Հասանելի են ինտերակտիվ վեցանկյուն սառցե կառուցվածքներ։
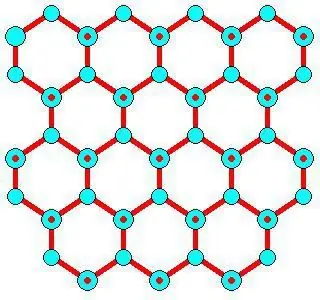
Զարգացման առանձնահատկություններ
Սառույցի ձևավորման համար անհրաժեշտ ջրի մոլեկուլների նվազագույն քանակը մոտավորապես 275 ± 25 է, ինչպես 280-ի ամբողջական իկոսաեդրային կլաստերի դեպքում: Ձևավորումը տեղի է ունենում 10 10 արագությամբ: օդ-ջուր միջերես և ոչ մեծ քանակությամբ ջրի մեջ: Սառցե բյուրեղների աճը կախված է տարբեր աճի տեմպերիցէներգիաներ. Կենսաբանական նմուշների, սննդի և օրգանների կրիոպահպանման ժամանակ ջուրը պետք է պաշտպանված լինի սառցակալումից։
Սա սովորաբար ձեռք է բերվում սառեցման արագ տեմպերով, օգտագործելով փոքր նմուշներ և կրիոկոնսերվատոր, ինչպես նաև մեծացնում է ճնշումը սառույցի միջուկի ձևավորման և բջիջների վնասումը կանխելու համար: Սառույցի/հեղուկի ազատ էներգիան աճում է ~30 մՋ/մ2-ից մթնոլորտային ճնշման դեպքում մինչև 40 մՋ/մ-2 200 ՄՊա-ի դեպքում՝ ցույց տալով. պատճառը, թե ինչու է այս ազդեցությունը տեղի ունենում:
Ինչ տեսակի բյուրեղային ցանց է բնորոշ սառույցին
Այլընտրանքն է, որ դրանք կարող են ավելի արագ աճել պրիզմայի մակերևույթներից (S2) արագ սառեցված կամ հուզված լճերի պատահականորեն խանգարված մակերեսի վրա: {1 1 -2 0} երեսներից աճը առնվազն նույնն է, բայց դրանք վերածում է պրիզմայի հիմքերի: Սառցե բյուրեղի զարգացման վերաբերյալ տվյալները ամբողջությամբ հետազոտվել են։ Տարբեր դեմքերի տարրերի հարաբերական աճի տեմպերը կախված են հոդի խոնավացման մեծ աստիճանի ձևավորման կարողությունից: Շրջապատող ջրի ջերմաստիճանը (ցածր) որոշում է սառցե բյուրեղի ճյուղավորման աստիճանը։ Մասնիկների աճը սահմանափակվում է գերսառեցման ցածր աստիճանի դիֆուզիայի արագությամբ, այսինքն՝ <2 ° C, ինչի արդյունքում դրանք ավելի շատ են:

Բայց սահմանափակվում է զարգացման կինետիկայով >4°C դեպրեսիայի ավելի բարձր մակարդակներում, ինչը հանգեցնում է ասեղի աճի: Այս ձևը նման է չոր սառույցի կառուցվածքին (ունի վեցանկյուն կառուցվածքով բյուրեղյա վանդակ), տարբեր.մակերևույթի զարգացման բնութագրերը և շրջակա (գեր-սառեցված) ջրի ջերմաստիճանը, որը գտնվում է ձյան փաթիլների հարթ ձևերի հետևում:
Մթնոլորտում սառույցի առաջացումը խորապես ազդում է ամպերի ձևավորման և հատկությունների վրա: Feldspars-ը, որը հայտնաբերված է անապատի փոշու մեջ, որը մթնոլորտ է ներթափանցում տարեկան միլիոնավոր տոննաներով, կարևոր ձևավորողներ են: Համակարգչային սիմուլյացիաները ցույց են տվել, որ դա պայմանավորված է պրիզմատիկ սառցե բյուրեղների հարթությունների միջուկացումով բարձր էներգիայի մակերեսային հարթությունների վրա:
Մի քանի այլ տարրեր և վանդակաճաղեր
Լուծված նյութերը (բացառությամբ շատ փոքր հելիումի և ջրածնի, որոնք կարող են ներթափանցել միջանցքներ) չեն կարող ընդգրկվել Ih կառուցվածքում մթնոլորտային ճնշման դեպքում, բայց դուրս են մղվում դեպի մակերես կամ ամորֆ շերտ՝ մասնիկների միջև։ միկրոբյուրեղային մարմին: Չոր սառույցի վանդակավոր տեղամասերում կան մի քանի այլ տարրեր՝ քաոտրոպիկ իոններ, ինչպիսիք են՝ NH4 + և Cl -, որոնք ներառված են ավելի թեթեւ հեղուկի սառեցման մեջ, քան մյուս կոսմոտրոպները, ինչպիսիք են Na + և SO42-, ուստի դրանք հեռացնելը հնարավոր չէ այն պատճառով, որ դրանք բյուրեղների միջև մնացած հեղուկից բարակ թաղանթ են կազմում: Սա կարող է հանգեցնել մակերևույթի էլեկտրական լիցքավորման՝ մակերևութային ջրի դիսոցիացիայի պատճառով, որը հավասարակշռում է մնացած լիցքերը (որը կարող է նաև հանգեցնել մագնիսական ճառագայթման) և մնացորդային հեղուկ թաղանթների pH-ի փոփոխության, օրինակ՝ NH 42SO4 դառնում է ավելի թթվային, իսկ NaCl-ը դառնում է ավելի հիմնային:
Դրանք ուղղահայաց են դեմքերինսառույցի բյուրեղյա վանդակ, որը ցույց է տալիս հաջորդ շերտը կցված (սև O ատոմներով): Դրանք բնութագրվում են դանդաղ աճող բազալ մակերեսով {0 0 0 1}, որտեղ կցված են միայն մեկուսացված ջրի մոլեկուլները: Պրիզմայի արագ աճող {1 0 -1 0} մակերես, որտեղ նոր կցված մասնիկների զույգերը կարող են կապվել ջրածնի հետ (մեկ ջրածնային կապ/տարրի երկու մոլեկուլ): Ամենաարագ աճող դեմքը {1 1 -2 0} է (երկրորդային պրիզմատիկ), որտեղ նոր կցված մասնիկների շղթաները կարող են փոխազդել միմյանց հետ ջրածնային կապի միջոցով: Նրա շղթաներից/տարրի մոլեկուլը ձև է, որը ձևավորում է գագաթներ, որոնք բաժանում և խրախուսում են փոխակերպումը պրիզմայի երկու կողմերին:
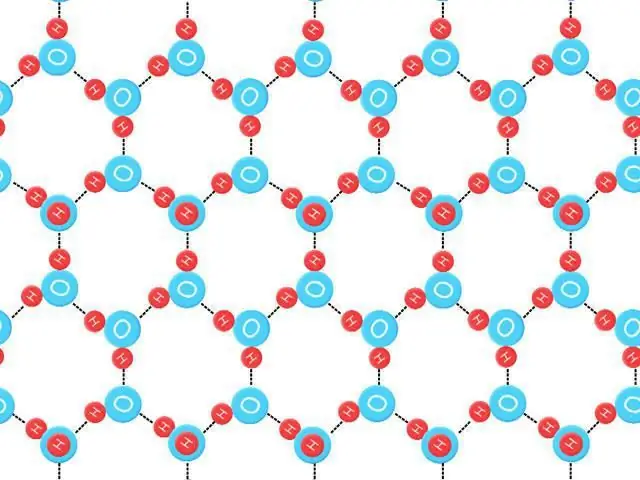
Զրոյական կետի էնտրոպիա
Կարելի է սահմանվել որպես S 0=k B ˣ Ln (N E0), որտեղ k B-ը Բոլցմանի հաստատունն է, NE-ը E էներգիայի կոնֆիգուրացիաների թիվն է, իսկ E0-ն ամենացածր էներգիան է: Վեցանկյուն սառույցի էնտրոպիայի այս արժեքը զրոյական Կելվինի վրա չի խախտում թերմոդինամիկայի երրորդ օրենքը «Իդեալական բյուրեղի էնտրոպիան բացարձակ զրոյում ուղիղ զրոյական է», քանի որ այս տարրերն ու մասնիկները իդեալական չեն, ունեն ջրածնային կապի անկարգություններ։
Այս մարմնում ջրածնային կապը պատահական է և արագ փոփոխվող: Այս կառույցները էներգիայով լիովին հավասար չեն, բայց տարածվում են շատ մեծ թվով էներգետիկ մոտ վիճակների վրա, ենթարկվում են «սառույցի կանոններին»։ Զրոյական կետի էնտրոպիան այն խանգարումն է, որը կմնա նույնիսկ, եթե նյութը կարողանար սառեցնել մինչև բացարձակզրո (0 K=-273, 15 ° C): Առաջացնում է փորձնական շփոթություն վեցանկյուն սառույցի համար 3, 41 (± 0, 2) ˣ mol -1 ˣ K -1: Տեսականորեն հնարավոր կլինի շատ ավելի մեծ ճշգրտությամբ հաշվարկել հայտնի սառցե բյուրեղների զրոյական էնտրոպիան (անտեսելով արատները և էներգիայի մակարդակի տարածումը), քան այն փորձարարականորեն որոշելը։
Գիտնականները և նրանց աշխատանքը այս ոլորտում
Կարելի է սահմանվել որպես S 0=k B ˣ Ln (N E0), որտեղ k B-ը Բոլցմանի հաստատունն է, NE-ը E էներգիայի կոնֆիգուրացիաների թիվն է, իսկ E0-ն ամենացածր էներգիան է: Վեցանկյուն սառույցի էնտրոպիայի այս արժեքը զրոյական Կելվինի վրա չի խախտում թերմոդինամիկայի երրորդ օրենքը «Իդեալական բյուրեղի էնտրոպիան բացարձակ զրոյում ուղիղ զրոյական է», քանի որ այս տարրերն ու մասնիկները իդեալական չեն, ունեն ջրածնային կապի անկարգություններ։
Այս մարմնում ջրածնային կապը պատահական է և արագ փոփոխվող: Այս կառույցները էներգիայով լիովին հավասար չեն, բայց տարածվում են շատ մեծ թվով էներգետիկ մոտ վիճակների վրա, ենթարկվում են «սառույցի կանոններին»։ Զրոյական կետի էնտրոպիան այն խանգարումն է, որը կմնա նույնիսկ, եթե նյութը կարողանար սառեցնել մինչև բացարձակ զրոյի (0 K=-273,15°C): Առաջացնում է փորձնական շփոթություն վեցանկյուն սառույցի համար 3, 41 (± 0, 2) ˣ mol -1 ˣ K -1: Տեսականորեն հնարավոր կլինի շատ ավելի մեծ ճշգրտությամբ հաշվարկել հայտնի սառցե բյուրեղների զրոյական էնտրոպիան (անտեսելով արատները և էներգիայի մակարդակի տարածումը), քան այն փորձարարականորեն որոշելը։

Չնայած մեծածավալ սառույցում պրոտոնների կարգը դասավորված չէ, մակերեսը, հավանաբար, նախընտրում է այս մասնիկների կարգը կախված H-ատոմների և O-զույգերի ժապավենների տեսքով (զրո էնտրոպիա կարգավորված ջրածնային կապերով): Գտնվել է զրոյական կետի խանգարումը ZPE, J ˣ mol -1 ˣ K -1 և այլն: Վերոնշյալ բոլորից պարզ և հասկանալի է, թե բյուրեղյա ցանցերի որ տեսակներն են բնորոշ սառույցին։






